Novozymes prisvinder 2017 og Nobelpristager 2020 Emmanuelle Charpentier var en af hovedkræfterne bag forvandlingen af bakteriernes immunsystem til det genteknologiske vidunderværktøj CRISPR-Cas, der kan kurere genetiske sygdomme. Selv mener hun dog slet ikke at have nået sine mål. Bakterier udgør nemlig en uudtømmelig ressource af viden og redskaber til at hjælpe os mennesker.
Bakterier kan sammenlignes med Dr. Jekyll og Mr. Hyde. Bedst som vi tror, at vi kender dem, overrasker de os allermest. Bakterier kan, når de er værst, dræbe mennesker. Når de er allerbedst, skaber de derimod større sundhed, fx i vores tarmes mikrobiom. Emmanuelle Charpentier har viet sit liv til at lære at forstå fundamentale spørgsmål om bakteriernes fysiologi.
Den mission førte hende til bakteriernes immunsystem, CRISPR-Cas og til udviklingen af dette til et genteknologisk vidunderværktøj.
"Bakterier har altid fascineret mig. Den ufattelige diversitet, der findes i bakteriernes verden, er et vidnesbyrd på, hvordan evolution virker i praksis. Der er et utal af forskellige typer. Dem der gør os syge, og dem der hjælper os. Betydningen af at forske i bakterier er derfor uvurderlig, for hvordan skal vi ellers kunne bekæmper multiresistente bakterier, og hvordan kan vi lære at bruge bakteriers værktøjer som fx CRISPR-Cas til gavn for os?" fastslår",="" serif;="" font-size:="" 20px;"=""> Emmanuelle Charpentier, direktør for Max Planck Institute for Infection Biology i Berlin.
Emmanuelle Charpentier har haft en omskiftelig forskertilværelse og oplevet forskerverdenen fra både de gode og mindre gode sider. Hun har kæmpet 20 år for at opnå anerkendelse fra en forskerverden, der synes hun zappede for meget rundt mellem universiteter og forskningsområder.
Det har været vigtigt for mig at følge min mavefornemmelse hele vejen igennem. Fra starten af troede jeg, at jeg som professorerne på mit institut skulle finde mit eget forskningsområde, som jeg kunne forske i resten af min karriere, men jeg fandt langsomt ud af, at det ikke var et bestemt emne, jeg søgte. Det, der har været den røde tråd gennem hele min karriere, har været at arbejde i krydsfeltet mellem grundforskning, klinisk forskning og anvendt forskning.Det jeg gør skal være nyt, og så skal det gøre en forskel.Med opdagelsen af CRISPR-Cas fik Emmanuelle Charpentier al den anerkendelse, hun havde søgt – og mere til, for med fundet og successen, fulgte kampen for at komme videre - til de mange opdagelser, der venter på hende.
Drømmen om at gøre en forskel
Jagten på at afsløre bakteriernes hemmeligheder starter på Pasteur-Instituttet i Frankrig, hvor Emmanuelle Charpentier som ung forsker hos professor Patrice Courvalin var blandt de allerførste at arbejde med den antibiotikaresistens, der i dag udgør en tikkende bombe under alle verdens sundhedssystemer. Dengang virkede de fleste antibiotika stadig, hvorfor fundet af multiresistente Listeria-bakterier var et stort chok. Bakterierne kan nemlig forårsage såvel meningitis som blodforgiftning hos nyfødte og ældre.
"Når man som ungt menneske, står med en prøve fra et 84 år gammelt menneske, der er truet på livet af multiresistente bakterier, får man et stort ønske om at kunne gøre en forskel. Det var her min interesse for såvel bakteriernes fysiologi som for den kliniske forskning blev vakt. Hvordan opstod resistensen og hvordan kunne vi udvikle en terapi?"
Charpentier og Courvalin viste som nogle af de første, at bakterier overførte disse resistensgener ikke bare fra bakterie til bakterie men faktisk mellem bakterietyper. Således arvede Listeria-bakterierne resistensgener fra andre bakterie-typer i det menneskelige tarmsystem. Så bakterietyperne kan altså aflure hinandens trick til at modstå bestemte typer af bakterier.
"Selvom min interesse allerede der var vakt for bakterier, klinisk forskning og udvikling af behandling, vidste jeg godt, at der ikke uden videre var plads til mig på Pasteur-Instituttet. Jeg regnede med, at jeg ligesom min professor skulle finde mit eget forskningsfelt og tog derfor ud i verden. Vi fandt ud af, at hvis jeg tog til USA og gjorde mig til ekspert i steptokokker, kunne jeg komme tilbage og starte min egen forskergruppe indenfor dette felt."
Det første store gennembrud
I 1996 tog Charpentier til Elaine Tuomanens laboratorium ved Rockefeller University i New York og derefter til St. Jude Children Research Hospital i Memphis med det formål at lære streptokokkernes verden bedre at kende. Streptokokker var og er et om end endnu større og mere udbredt problem i sundhedssystemet end Listeria-bakterier. Det var dog noget helt andet, der først og fremmest bjergtog Charpentier ved den amerikanske forskerverden, da hun ankom.
"Det var dybt inspirerende at opleve hele starten af den store bioteknologiske satsning, der prægede USA fra mid-halvfemserne og frem. Når man som medicinsk mikrobiolog kom fra den mere konservative europæiske forskerverden, var det utroligt at se, hvordan forskerverdenen i USA på ingen tid lykkedes med at bygge bro fra den akademiske universitetsverden til den farmaceutiske industri."
Charpentiers forskning nåede nye højder hos professor Elaine Tuomanen, hvis forskning blandt andet havde fokus på livstruende steptokoksygdomme hos børn. Hidtil havde antibiotikummet vancomycin været sidste bastion i kampen mod bakterier, og forskerne vidste, at der ventede en katastrofe, hvis også det antibiotika holdt op med at virke. Forskernes fund af, hvilke molekylære mekanismer i steptokokker, der førte til vancomycin-restistens landede derfor i verdens fornemste tidsskrift Nature.
Der er ingen tvivl om, at jeg har haft det rette held og næse for at finde de bedste mentorer, og hver af dem har haft en stor betydning for min karriere. Samtidig har kombinationen af det grundvidenskabelige og det anvendte altid været drivkraften for mig. Og endelig har det været vigtigt for mig ikke at gro fast men finde det næste store projekt, hvor jeg kunne gøre en forskel.Inden Charpentier bevægede sig videre, lykkedes det dog forskerne også at afsløre afgørende omkring antibiotikas mekanismer. De fandt nemlig frem til, at antibiotika som fx penicillin ikke direkte forårsager bakteriers død, men at antibiotika først er nødt til at igangsætte en selvmordsproces hos bakterierne. En proces der i sidste ende fører til, at bakterierne opløser deres egen cellevæg og dør.
Svært at forblive i den akademiske verden
Selv om Charpentier egentlig havde planlagt at skulle tilbage til Europe efter opholdet i USA, var hun forbi midlertidige stillinger på både Rockefeller University, New York University Langone Medical Center, Skirball Institute of Biomolecular Medicine i New York, inden hun tog retur, og trods den store succes i USA, var det ikke ligefrem faste job i den akademiske verden, der ventede hende i Europa, da hun vendte tilbage i 2002.
"Det var som om der blev kigget skævt til min karriere, fordi den ikke havde været fokuseret på et bestemt emne, men nærmere på en måde at forske på, hvor man havde øje både for det grundvidenskabelige og det anvendte – mellem det akademiske og det industrielle. Samtidig var jeg vant til fra USA at have friheden til at starte noget nyt, hvorimod den europæiske forskerverden var langt mere gammeldags dengang."
Selv om Charpentier en overgang overvejede at søge mod industrien, endte hun med at blive ansat som junior group leader på University of Vienna, hvor hun kunne få relativt frie hænder til at bygge en forskningsgruppe op. Af forskellige årsager, blev hun interesseret i det spirende forskningsområde indenfor den regulerende rolle i bakterier af - DNAs kemiske kusine - RNA. Hun satte sig for at opdage og karakterisere RNA-molekylerne i streptokokker.
"Det var tydeligt fra forskningen, at RNA-molekylerne måtte en væsentlig rolle for bakteriernes måde at regulere sig selv på. For eksempel var det blevet vist, at RNA-molekyler påvirker både transkription af DNA til RNA og translation af RNA til protein. Meget lidt var dog kendt om RNA-biologien i den patogene bakterie Streptococcus pyogenes, og jeg mente nok, at der var en god chance for finde nye mekanismer der. Så det virkede som et godt emne at bygge et nyt laboratorium op omkring."
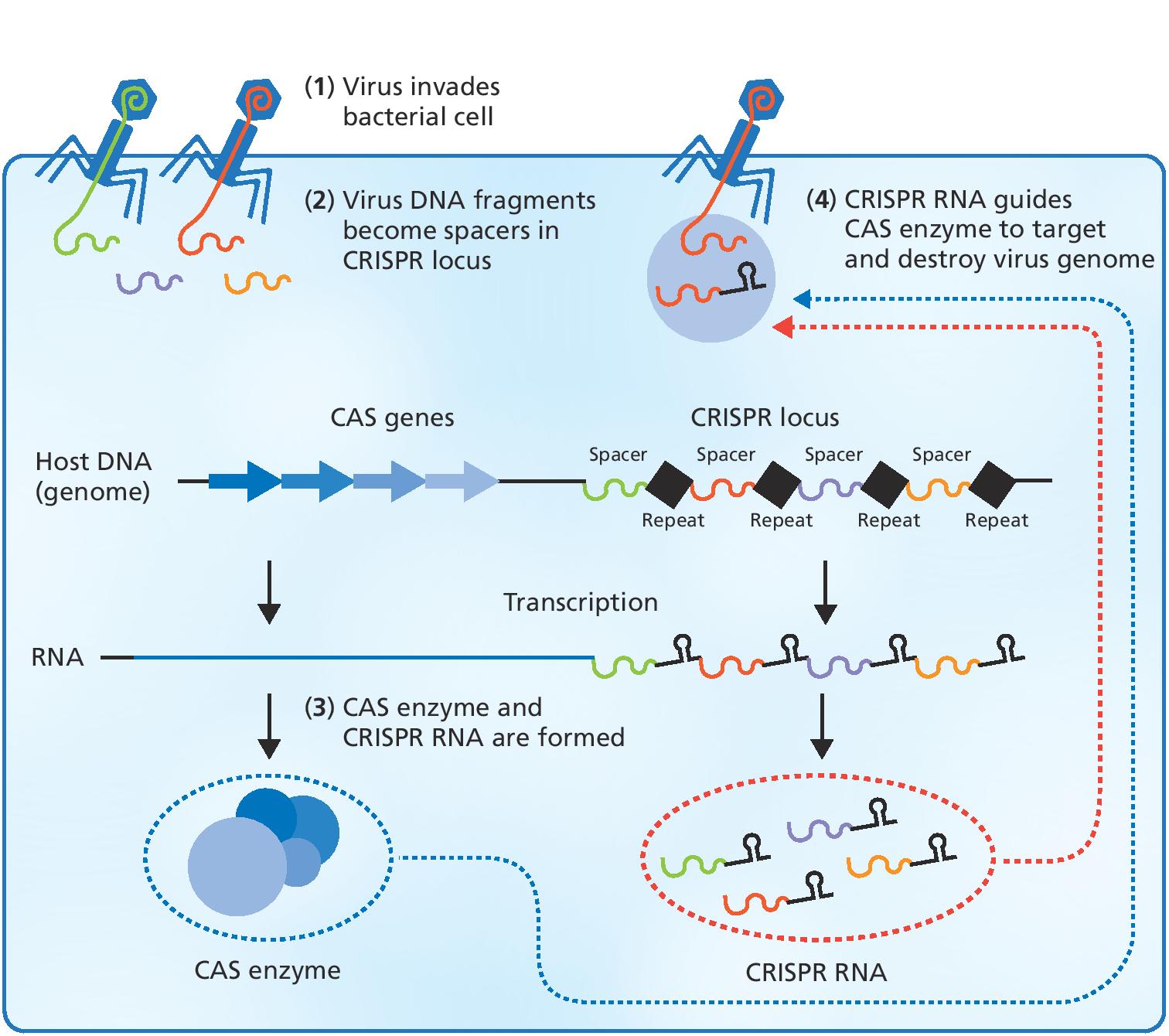
Detect and destroy
Snart fandt Charpentiers gruppe frem til, at et RNA-molekyle, der havde betydning fra streptokokkers evne til at angribe, og i arbejdet med RNA-molekylerne, faldt Charpentier over artikler om bakteriers eget immunsystem, CRISPR, der berettede om, at bakterier klipper små DNA-stykker fra angribende virus, indarbejder dem i deres genom, så de kan huske virus DNA-sekvenser igen, når de bliver angrebet. En slags genetisk vaccinationskort om man vil.
Det der for alvor fangede Charpentiers opmærksomhed var, at bakterierne sender RNA-kopier ud i cellen af de DNA-stykker, den tidligere har kopieret fra en indtrængende virus. Hvis de binder sig til en DNA-sekvens i cellen, ved cellen, at det er en indtrængende virus, der skal destrueres.
Charpentier havde i mellemtiden startet nyt laboratorium på Laboratory for Molecular Infection Medicine Sweden, Umeå, Sweden. I 2006 screenede hun og hendes team S. pyogenes og fandt talrige nye små RNA-typer, og det gav forskerne en stor overraskelse.
"Vi fandt de små CRISPR RNA-molekyler med sekvenser, der var identiske med de virus-sekvenser, som bakterierne var stødt på undervejs. Hvad der forbavsede os var imidlertid et andet RNA-molekyle, der der også havde en bemærkelsesværdig lighed med CRISPR RNA."
Det Charpentier og hendes kollegaer havde fundet var den sidste brik i det CRISPR-Cas-systemet. Når man blandede crRNA og Cas-proteinet med de nye RNA-stykker (transacting RNA) i et reagensglas, havde man et fuldt funktionelt bakterielt immunforsvar, der kunne tilintetgøre virus.
Som en smartphone
Med Charpentiers fund af transacting RNA startede et intenst kapløb. CRISPR-Cas-systemet viste sig at være så enkelt og elegant at arbejde med, at det inden længe skulle blive allemandseje. Først skulle Cas-proteinets funktion dog afklares. Det tog ikke forskerne længe at gætte, at Cas var et enzym, der som en saks kunne klippe indtrængende virus-DNA i stykker.
",="" serif;="" font-size:="" 20px;"="">"Sammen med Jennifer Doudna opdagede vi, at man blot ved at ændre CRISPR RNA-sekvensen kunne omprogrammere Cas9-enzymet til at skære ved en korresponderende DNA-sekvens. Det er et utrolig smukt design, og næsten lige så elegant som en smartphone - enkel og brugervenlig, men ikke desto mindre både alsidig og sofistikeret. Da vi så det, vidste vi, at vi havde opdaget et genteknologisk værktøj, der overgik alt, vi tidligere havde set."
CRISPR-Cas blev den revolution som Charpentier forudsagde. Det viste sig nemlig, at systemet nemt kunne overføres fra bakterier til mennesker. Dermed kunne systemet benyttes til at reparere i det menneskelige genom, og få CRISPR-Cas til at klippe fejlbehæftede gensekvenser ud og erstatte dem med nye.
Talk of the town
Overnight blev CRISPR-Cas talk of the town, og Emmanuelle Charpentier fik al den anerkendelse hun aldrig tidligere havde fået – og mere til. Sammen med sin amerikanske kollega Jennifer Doudna blev hun berømmet og blev blandt andet sat på Time Magazines Top 100-listen over de mest indflydelsesrige personer i verden. Samtidig begyndte den videnskabelige anerkendelse også at strømme ind.
"Jeg havde aldrig tidligere været en del af den videnskabelige elite og har aldrig haft noget særligt behov for at være der, men jeg vidste godt allerede i 2012, da jeg første gang sagde ja til at modtage en videnskabelig pris fra CRISPR-Cas, at det nok ikke ville blive den sidste. En af mine venner sagde til mig: Du bør tage imod den, for hvis du ikke modtager den, står der helt sikkert en anden i kulissen klar til at tage æren."
Fra 2014 har Charpentier modtaget ikke mindre end 40 store videnskabelige priser og medaljer inkl. store priser the Warren Alpert Foundation Prize, the Gruber Foundation International Prize og the Breakthrough Prize in Life Sciences. Hun er ligeledes af flere omgange nævnt som kandidat til Nobelprisen. Selv om hun er stolt og glad for hver eneste pris, så er det altid med en vis påpasselighed, at hun tager imod.
"En pris som Novozymes-prisen har utrolig stor betydning for mig, fordi det er folk fra et andet forskningsfelt – nemlig det bioteknologiske – der har kigget på mit arbejde og sagt, at det har haft stor betydning for deres. Derfor ser jeg først og fremmest prisen som en pris til mit eget felt – mikrobiologien – og som en anerkendelse af vigtigheden af den forskning."
Trying to escape CRISPR
Netop betydningen af mikrobiologien og jagten på nye anvendelser af viden om de bakterielle systemer til gavn for mennesker fylder rigtig meget i Charpentiers hverdag i disse år. CRISPR har nemlig fyldt alt de sidste 6 år, og frygten for at den skulle overtage alt, har derfor også præget hendes overvejelser. Med op til 20 priser årligt og hvad der følger med af interviews og rejser, er det vigtigt at bevare fokus.
"Der er utrolig mange distraktioner til at fjerne mit fokus fra det, jeg virkelig synes er vigtigt, nemlig videnskaben, og min frygt er at blive fanget i mit eget net og til evig tid være kendt som hende, der fandt CRISPR-Cas. Jeg føler dog, at der er meget mere, jeg skal nå at udrette, så derfor prøver jeg også at lægge CRISPR bag mig, vel vidende, at det lige nu ikke er muligt."
Hendes seneste job direktør for Max Planck Institute for Infection Biology i Berlin, som hun har bestredt siden 2016, har dog muliggjort, at hun kan lægge en vis distance til CRISPR-Cas, der i dag kun udgør en ud af fem forskningsområder. På den måde fylder CRISPR-Cas stadig mindre i hendes hverdag uden helt at forsvinde fra landkortet.
"Vi arbejder stadig med at forbedre CRISPR-Cas-værktøjet. Det største fremskridt vi har gjort, var det arbejde, som vi offentliggjort sidste år i Nature, hvor vi offentliggjorde fundet af et endnu simplere system fra bakterien Francisella novicida, hvor enzymet Cpf1 forener Cas-enzymet og tracrRNAs funktioner i et. Det betyder, at vi står med et endnu simplere og mere elegant system."
En fri elektron
Lige nu føler Emmanuelle Charpentier sig for første gang i sin karriere som en fri fugl eller som hun selv udtrykker det ”en fri elektron”, der kan bevæge sig frit rundt i bakteriernes skatkammer, hvor hun selv mener, at det er rigtigt.
”Bakterier er som værktøjsmagere. De koder for et stort udvalg af enzymer, der har revolutioneret biologier. Disse enzymer har gjort os i stand til at læse hele genomer, herunder det humane genom. De producerer enzymer, som kan spalte og sætte DNA-molekyler sammen igen. De har muliggjort kloning. Med CRISPR-Cas-systemet har de leveret endnu et værktøj - den gang til at lave gen-kirurgi, der kan reparere genetiske mutationer."
Den næste store udfordring er at få CRISPR-Cas-systemet til at fungere i de rigtige væv, så gener kan blive repareret de helt rigtige steder, uanset om det er i hjernen, hjertet eller endnu et sted. For Emmanuelle Charpentier er CRISPR-Cas dog blot en af mange værktøjer, der skal arbejdes med på hendes nye institution.
"Udover vores fortsatte studier af CRISPR, undersøger vi også de små regulatoriske RNA, der er væsentlige for bakteriers patogenicitet og mekanismerne vores immunsystems genkendelse af bakterier. Den fortsatte søgen i bakterier vil helt sikkert afsløre nye typer af enzymer, der vil være meget nyttige for gen-redigering. Og med den voksende antibiotikaresistens, er der bestemt også behov for bedre at forstå, hvordan smitsomme sygdom forårsages af bakterier. "
Vigtigst for Charpentier er dog hendes fortsatte arbejde med at uddanne unge forskere til at sikre videnskabens fremtid. Store donationer fra både Kempe- and Wallenberg-fondene har givet hende mulighed for at træne endnu flere unge forskere
"At arbejde med unge studerende er den mest inspirerende del af jobbet og ekstremt vigtigt for det videnskabelige samfund. Jeg forsøger at lære dem det, der har været vigtigst for min karriere og min forskning. Det er at følge sin mavefornemmelse, tro på sine ideer og have et åbent sind for nye ideer. Uden et åbent sind, havde jeg aldrig fundet CRISPR-Cas. "
Nobelprisen i kemi er tildelt Emmanuelle Charpentier og Jennifer A. Doudna. Novozymes Prisen 2017 blev fredag d. 17. marts 2017 uddelt til Professor Emmanuelle Charpentier, Department of Regulation in Infection Biology, Max Planck Institute for Infection Biology, Berlin, Tyskland, og Professor Virginijus Siksnys, , Institute of Biotechnology, Vilnius University, Litauen.
